Purification engineering technology research center of Sichuan Province Natural Medicine
四川省天然药物分离纯化工程技术研究中心
公司要闻
天然花青素C3G的多靶点药理活性研究进展
本文来自: 发布时间:2025-09-25
矢车菊素-3-O-葡萄糖苷(Cyanidin-3-O-glucoside,C3G)作为一种广泛存在于水果、蔬菜和谷物中的天然花青素,因其鲜艳的色泽和多样的生物活性而备受关注。本文概述了矢车菊素-3-O-葡萄糖苷近期在抗氧化、抗炎、抗癌、代谢调节和器官保护等方面的研究进展,并对其作用机制、生物利用度和稳定性改善策略进行总结,旨在为其开发应用提供理论支撑及实物支持。
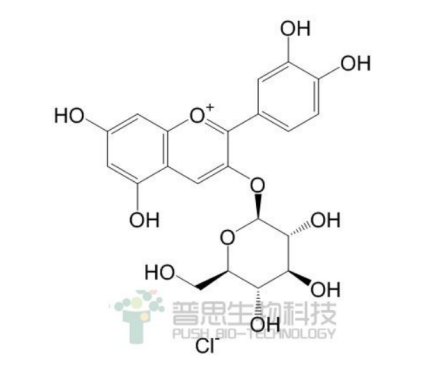
英文名:Cyanidin 3-O-glucoside chloride
中文名:矢车菊素-3-O-葡萄糖苷
CAS号:7084-24-4
分子式:C21H21ClO11
分子量:484.84g/mol
结构类型:Anthocyanins
来源:桑叶、越桔、番薯、蓝莓、黑米
溶解度:溶于甲醇、水、氯仿
LogP:0.19
中文副名:氯化紫菀苷,氯化白除虫菊苷
英文副名:Kuromanin,Kuromanine,Cyanidin 3-β-glucoside,Glucocyanidin,Chrysontemin
一、抗炎活性[1]
研究发现:
C3G及其脂质体在THP-1巨噬细胞中显著降低多种炎症相关因子(TNF-α,IL-1β,IL-6,IL-8)的水平,并保护细胞免于凋亡。
作用机制:
抑制LPS诱导的NF-κB信号通路活化,从而减少促炎细胞因子的释放(图1)。
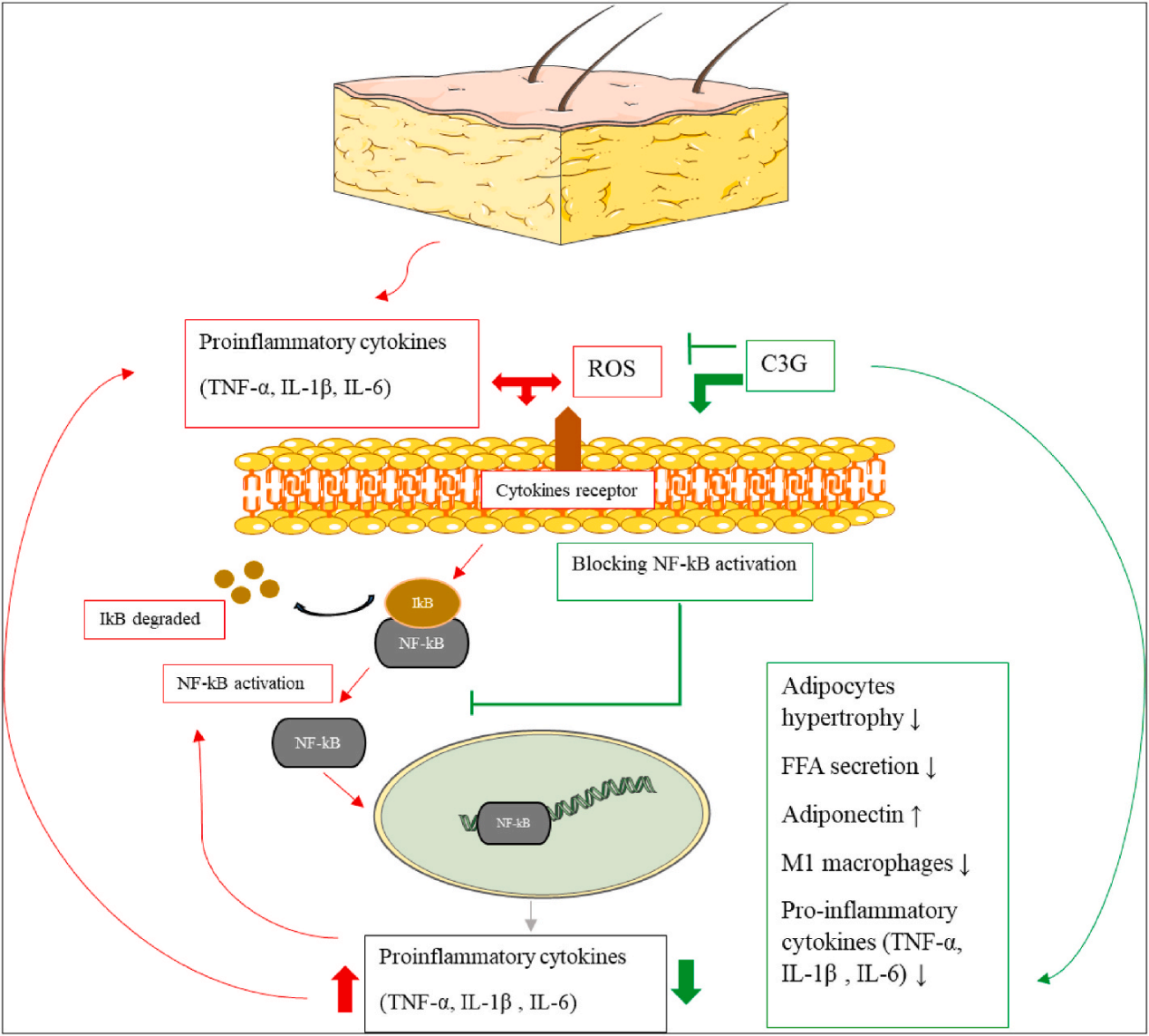
图1 矢车菊素-3-O-葡萄糖苷(C3G)作为抗炎剂的作用机制[9]
二、抗氧化活性[2]
研究发现:
C3G脂质体能显著提升GES-1胃上皮细胞的总抗氧化能力(T-AOC),降低脂质过氧化产物MDA,保护细胞免受H2O2诱导的氧化损伤。
作用机制:
通过激活细胞内源性抗氧化通路,清除自由基,减轻氧化应激。
三、细胞保护(lncRNA调控)[3]
研究发现:
C3G能通过改变长链非编码RNA(lncRNA)的表达谱,减轻玉米赤霉烯酮(ZEN)对猪颗粒细胞的损伤。
作用机制:
调节lncRNA表达,干预PI3K/AKT信号通路,抑制细胞凋亡。
四、神经保护[4]
研究发现:
通过激活Nrf2信号、抑制GSK-3β、调节线粒体功能及抗氧化酶活性,在肾脏、视网膜、肺和神经系统中全面对抗氧化应激[1]。
作用机制:
在Aβ转基因线虫模型中抑制Aβ聚集,增强抗氧化能力,改善记忆。在BV2小胶质细胞中抑制LPS诱导的炎症和氧化损伤。
五、糖异生与癌细胞衰老[5]
研究发现:
C3G通过激活AMPK途径抑制肝脏糖异生,并能诱导氧化应激下的癌细胞衰老和凋亡。
作用机制:
激活AMPK通路,进而抑制糖异生(图2);通过诱导细胞衰老和凋亡发挥抗癌活性。
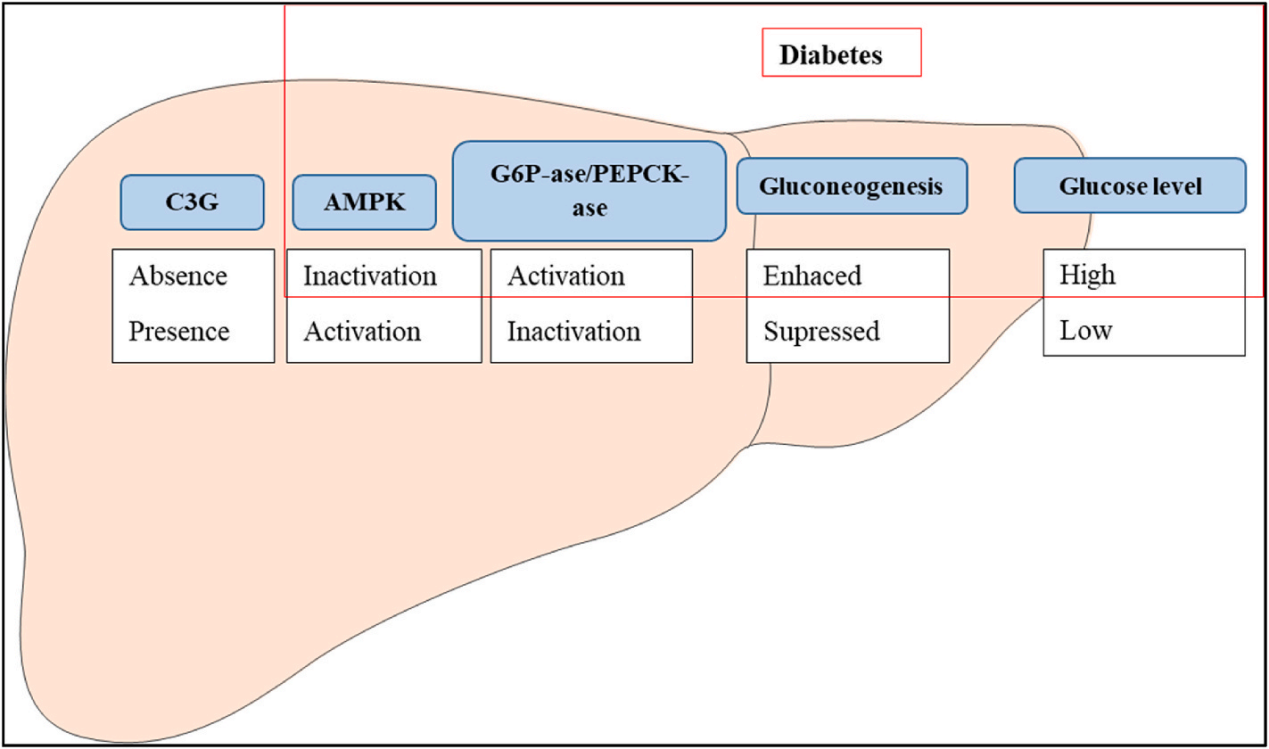
图2 矢车菊素-3-O-葡萄糖苷(C3G)在糖尿病中的调控机制
六、抗真菌毒素[6]
研究发现:
C3G能影响禾谷镰刀菌的生长并持续降低其产生的enniatin真菌毒素。
作用机制:
影响真菌生长和毒素生物合成。
七、酶抑制活性[7]
研究发现:
C3G对α-淀粉酶和α-葡萄糖苷酶表现出可逆的非竞争性抑制作用,提示其在血糖控制方面的潜力。
作用机制:
通过氢键和疏水力与酶的关键氨基酸残基相互作用,抑制碳水化合物消化酶活性。
1、女性生殖健康[8]
研究发现:
C3G对女性生殖健康有益,能保护卵巢细胞免受氧化应激,抑制卵巢癌和宫颈癌细胞生长,并可能缓解多囊卵巢综合征(PCOS)。
作用机制:
抗氧化、抗炎、诱导癌细胞凋亡、调节雌激素受体及相关生长因子和血管生成通路(图3)。
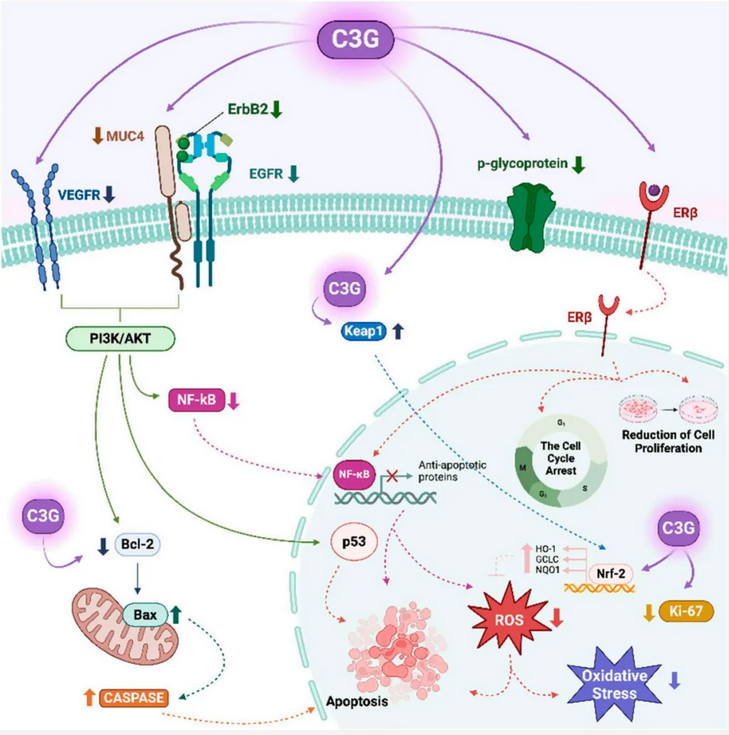
图3 矢车菊素-3-O-葡萄糖苷(C3G)通过多种细胞信号通路对女性生殖过程的凋亡效应[8]
2、调节代谢紊乱与预防肥胖[9]
研究发现:
C3G在预防肥胖相关代谢紊乱中功效显著,能调节脂质代谢、增强能量稳态,并改善心血管疾病、2型糖尿病及胰岛素抵抗。
作用机制:
调节脂质代谢、增强能量稳态、抗氧化、抗炎、抑制NF-κB通路、激活Nrf2/AMPK通路、改善肠道菌群(图4)。
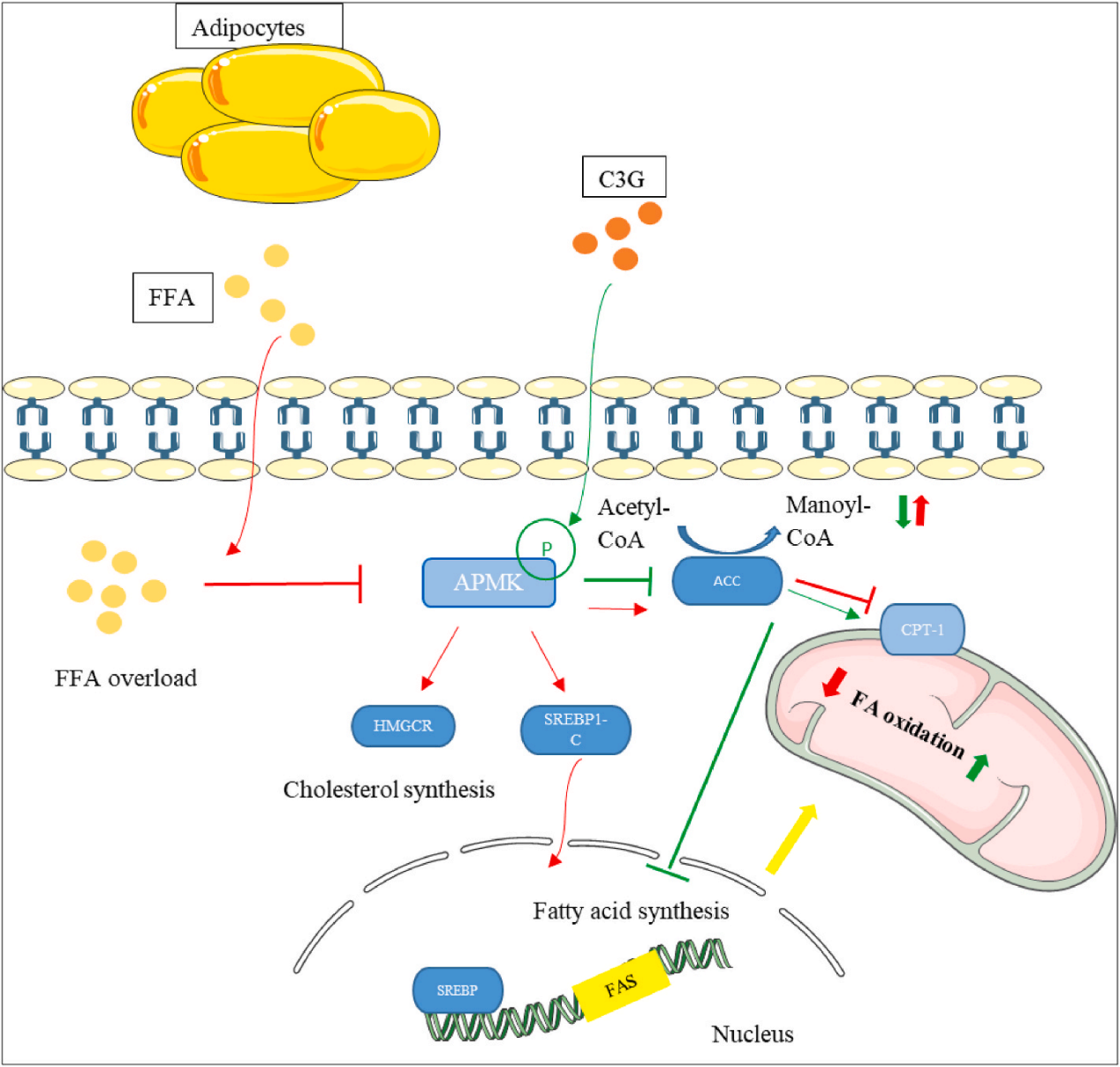
图4 矢车菊素-3-O-葡萄糖苷(C3G)调控脂质代谢示意图[9]
3、缓解运动性疲劳[10]
研究发现:
C3G等天然黄酮类化合物通过抗氧化和抗炎特性,在缓解运动性疲劳方面显示出潜力。
作用机制:
抑制氧化应激和炎症反应,调节能量代谢,激活Keap1/Nrf2/ARE和AMPK/PGC1-α通路。
4、肝脏保护[11]
研究发现:
C3G的酰化衍生物(C3G-月桂酸酯)对H2O2诱导的LO2肝细胞氧化损伤具有显著保护作用。
作用机制:
抑制活性氧产生,恢复抗氧化酶活性,改善线粒体功能,并激活PI3K/Akt-Nrf2-HO-1/NQO1通路。
5、肾脏保护[12]
研究发现:
黑米中的C3G能显著预防链脲佐菌素诱导的糖尿病大鼠的肾功能障碍和肾纤维化。
作用机制:
抗胰岛素抵抗、抗氧化应激、抗炎、抑制TGF-β1/p-Smads表达和细胞外基质(ECM)聚集。
6、畜牧业应用[13]
研究发现:
富含C3G的黑甘蔗青贮料可作为饲料,减轻山羊的氧化应激,并改善肉质。
作用机制:
调节瘤胃发酵,提高抗氧化酶活性,稳定肌肉膜,改善肉质。
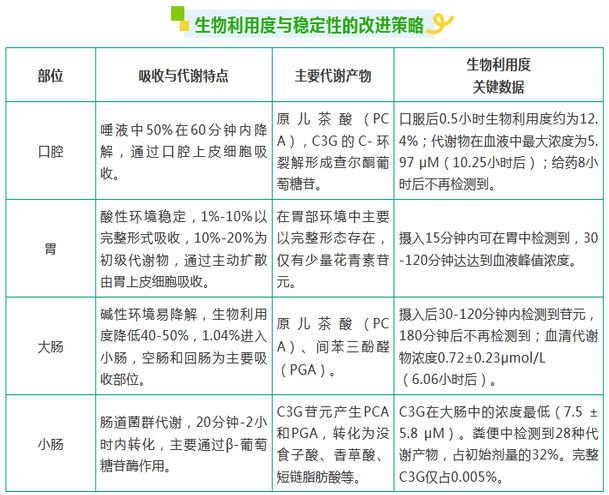
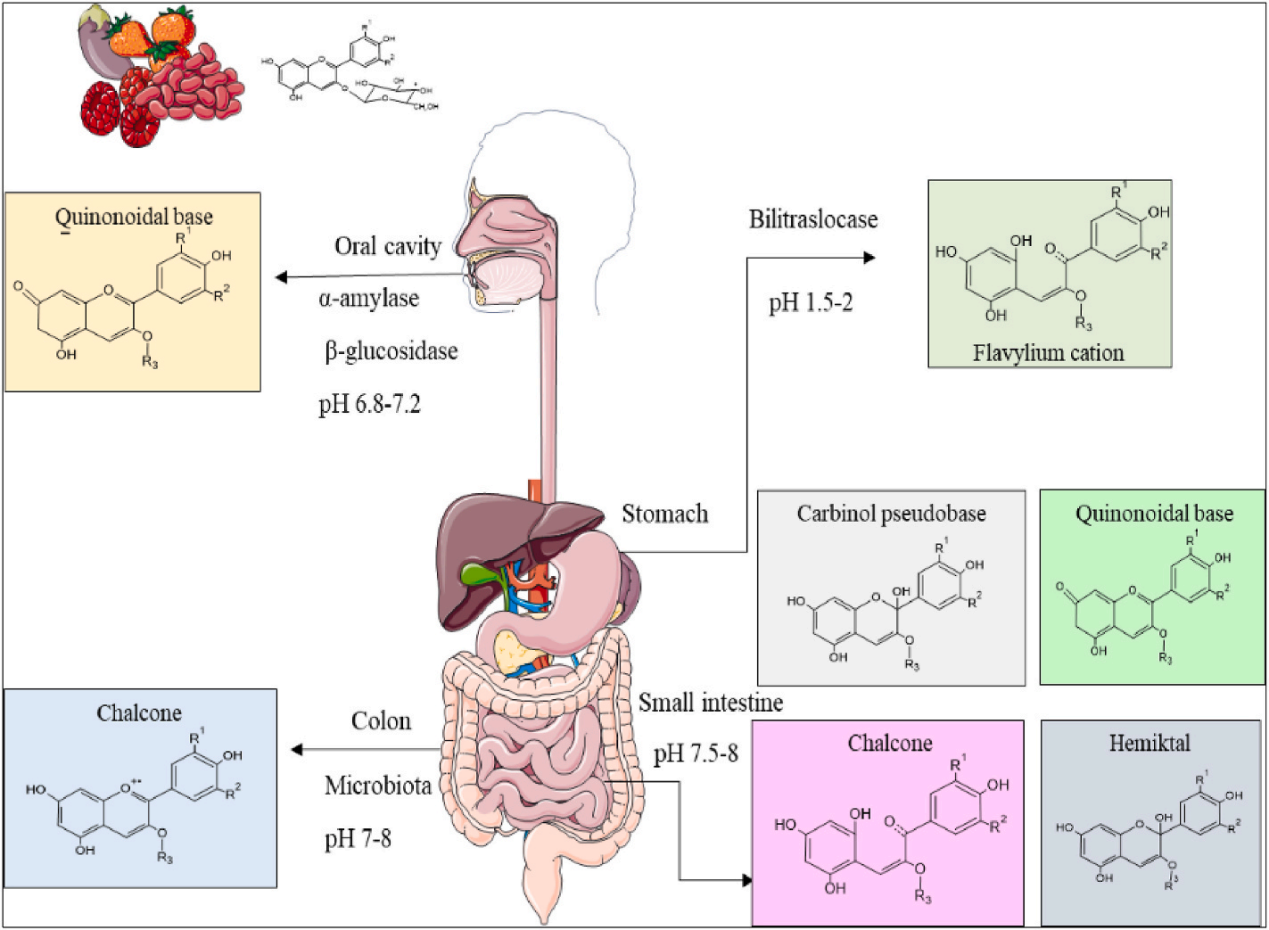
图5 矢车菊素-3-O-葡萄糖苷(C3G)在人体胃肠道不同部位的降解和吸收示意图[9]
C3G的临床应用潜力受到其理化性质的限制,主要是低稳定性和低生物利用度。近期的研究重点之一是开发新策略以克服这些挑战。
1、递送系统封装
脂质体和纳米脂质体作为递送载体,能有效提高C3G的稳定性、溶解度和生物利用度[1][2]。有研究表明,C3G脂质体粒径约为234nm,包封率可达75.0%,能显著提高其在GES-1细胞中的抗氧化活性[2]。
2、分子修饰
酶促酰化是一种有效的修饰方法。通过将脂肪酸链连接到C3G的葡萄糖部分,可以显著提高其亲脂性和稳定性[14]。研究发现,虽然酰化降低了C3G的体外抗氧化活性,但其细胞内抗氧化活性却显著增强,例如,C3G-月桂酰基酯的细胞抗氧化能力比C3G高出125.9%[14]。另一项研究也证实,C3G-月桂酸酯比C3G本身具有更优的肝保护作用[11]。
3、与大分子相互作用
C3G与食品基质中的大分子(如蛋白质和多糖)的相互作用也影响其稳定性。研究发现,C3G可以与酪蛋白水解物发生相互作用,并通过氢键、范德华力或疏水作用形成复合物[15]。这种相互作用在某些条件下表现出协同抗氧化效应,但也可能因掩盖活性基团而产生拮抗作用[15]。同样,与经过超声修饰的果胶结合,可以提高C3G的热稳定性[16]。然而,与β-伴大豆球蛋白(7S)的强相互作用在热处理后反而降低了C3G的生物可及性和抗氧化能力[17]。
普思生物可大量供应矢车菊素-3-O-葡萄糖苷,并可根据客户需求进行委托定制生产。

性状:固体
颜色:紫红色
储藏条件:密闭、干燥、常温
供应规格:克级至百克级供应,有成熟工艺,稳定供应
理化数据来源:普思生物官网、PubChem、HMDB
参考文献:
[1] Hao X, Guan R, et al. Anti‐inflammatory activity of cyanidin‐3‐O‐glucoside and cyanidin‐3‐O‐glucoside liposomes in THP‐1 macrophages[J]. Food Science & Nutrition, 2021, 9(12): 6480-6491.
[2] Quan Z, Guan R, et al. Antioxidant activity and absorption of cyanidin-3-O-glucoside liposomes in GES-1 cells in vitro[J]. Bioscience, Biotechnology, and Biochemistry, 2020, 84(6): 1239-1249.
[3] Li X, Zhang F, et al. LncRNA profiles of cyanidin-3-O-glucoside ameliorated zearalenone-induced damage in porcine granulosa cells[J]. Gene, 2023, 884: 147693.
[4] Zhu Z, Yang L, Li Z, et al. Cyanidin‐3‐O‐glucoside, cyanidin, and oxidation products of cyanidin protect neuronal function through alleviating inflammation and oxidative Damage [J]. Journal of Food Science, 2022, 87(5): 2159–2172.
[5] Jia Y, Wu C, Rivera-Piza A, et al. Mechanism of Action of Cyanidin 3-O-Glucoside in Gluconeogenesis and Oxidative Stress-Induced Cancer Cell Senescence [J]. Antioxidants, 2022, 11(4): 749.
[6] Felici L, Atanasova V, et al. Cyanidin 3-O-glucoside and other anthocyanins affect enniatins production in fusarium avenaceum[J]. Fungal Biology, 2025, 129(6): 101640.
[7] Wang W, Cui Y, Zheng M, et al. Inhibitory kinetics of cyanidin-3-O-glucoside against α-amylase and α-glucosidase. [Z](2023–09–06).
[8] Majerik Behinska K, Balkova E, Mihal M, Roychoudhury S, Kolesarova A. The therapeutic potential of cyanidin-3-O-glucoside relating to female reproductive health[J]. Frontiers in Pharmacology, 2025, 16.
[9] Oumeddour D, Al-Dalali S, Zhao L, Zhao L, Wang C. Recent advances on cyanidin-3-O-glucoside in preventing obesity-related metabolic disorders: A comprehensive review[J]. Biochemical and Biophysical Research Communications, 2024, 729: 150344.
[10] Liu Y, Shen X, Sha M, et al. Natural bioactive flavonoids as promising agents in alleviating Exercise-induced Fatigue [J]. Food Bioscience, 2023, 51: 102360.
[11] Zhou P, Pan Y, Yang W, et al. Hepatoprotective effect of Cyanidin-3-O-glucoside–lauric acid ester against H2O2-induced oxidative damage in LO2 Cells [J]. Journal of Functional Foods, 2023, 107: 105642.
[12] Qi S S, He J, Dong L C, et al. Cyanidin-3-glucoside from black rice prevents renal dysfunction and renal fibrosis in streptozotocin-diabetic Rats [J]. Journal of Functional Foods, 2020, 72: 104062.
[13] Suong N T M, Paengkoum S, Schonewille J T, et al. Growth Performance, Blood Biochemical Indices, Rumen Bacterial Community, and Carcass Characteristics in Goats Fed Anthocyanin-Rich Black Cane Silage [J]. Frontiers in Veterinary Science, 2022, 9.
[14] Zhang P, Liu S, Zhao Z, et al. Enzymatic acylation of Cyanidin-3-glucoside with fatty acid methyl esters improves stability and antioxidant Activity [J]. Food Chemistry, 2021, 343: 128482.
[15] Yin Z, Wu Y, Chen Y, et al. Analysis of the interaction between Cyanidin-3-O-glucoside and casein hydrolysates and its effect on the antioxidant ability of the Complexes [J]. Food Chemistry, 2021, 340: 127915.
[16] Luo F, Zhang Z, Lu F, et al. Ultrasound modification of pectin and the mechanism of its interaction with Cyanidin-3-O-Glucoside [J]. Food Hydrocolloids, 2024, 152: 109898.
[17] Qie X, Chen W, Wu Y, et al. Entrapment of Cyanidin-3-O-glucoside in β-conglycinin: From interaction to bioaccessibility and antioxidant activity under thermal Treatment [J]. Food Chemistry, 2023, 398: 133832.