Purification engineering technology research center of Sichuan Province Natural Medicine
四川省天然药物分离纯化工程技术研究中心
公司要闻
主峰纯度考察的终极解决方案 —2D-UPLC-QTOF技术
本文来自: 发布时间:2026-02-12
主峰纯度考察是药品研发与注册申报中的关键技术性研究项目,频繁出现在国家药品监督管理局药品审评中心(CDE)补充资料通知中,核心要求为对强制降解实验主峰开展纯度考察,并优先推荐采用质谱方法验证。
一、核心目的与监管逻辑
1. 强制降解实验的核心价值
强制降解实验(破坏性试验)的核心目标是验证分析方法的专属性与稳定性指示能力,即所建立的质量标准方法(多为HPLC-UV)在药物发生降解时,既能准确测定主成分含量,又能有效分离、检测出降解产物,为药品稳定性评价提供可靠依据。
2. 传统分析方法的局限性
传统主峰纯度检查依赖HPLC-UV/DAD的光谱一致性分析,但UV光谱易受共轭系统相似杂质干扰,无法区分共流出杂质。
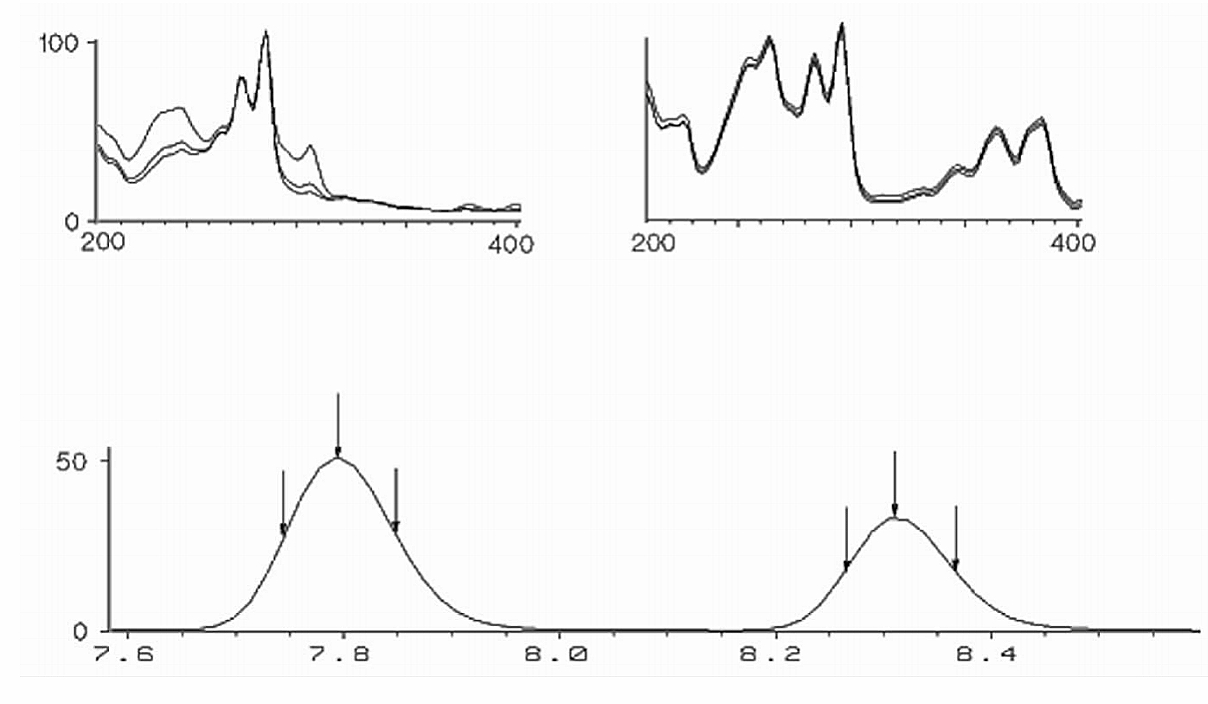
图1 2个色谱峰各自3个点的紫外光谱归一化比较峰纯度[1]
近年液质联用法虽逐步普及,但传统质谱技术仍存在明显短板,各类方法的差异与局限如下表所示。
分析方法 | 在纯度考察中的差异和局限 |
HPLC-UV/DAD | 无法分离共流出物,无杂质结构解析能力,DAD峰纯度检查易受干扰,假阳性风险高。 |
UPLC-MS(单四极杆) | 分辨率有限,对复杂基质中微量共流出杂质的区分能力不足,定性准确性欠佳。 |
一维UPLC-QTOF | 不适用含缓冲盐和离子对试剂的检测方法;依赖单一色谱分离机理,难以突破共流出杂质的保留时间重叠瓶颈,峰容量不足。 |
3. 监管机构发补的核心质疑
CDE审评的核心质疑点的是:强制降解条件(酸、碱、氧化、高温、光照)下,HPLC色谱图中看似单一的主峰是否为“真纯峰”。可能存在的隐患包括:降解杂质与主成分保留时间完全一致形成混合峰、主成分发生微小结构变化但色谱行为未改变。若存在共流出问题,HPLC含量测定结果将失真,稳定性指示方法的可靠性也会被否定,因此需高维度技术验证主峰纯度。
二、2D-UPLC-QTOF考察主峰纯度的核心内容
二维超高效液相色谱(2D-UPLC)与高分辨飞行时间质谱(QTOF)联用技术,凭借“正交分离+高分辨鉴定”的双重优势,成为强制降解实验主峰纯度考察的最优解决方案,可彻底回应CDE对色谱峰“表观纯度”的终极质疑。

1. 核心技术原理
该技术通过三级联动实现精准纯度验证,构建“分离-捕获-鉴定”的完整技术链条:
Ø 第一维分离:采用反相C18等色谱柱,基于组分极性对强制降解样品进行初步分离,通过中心切割模式捕获可能含共流出物的主峰馏分;
Ø 第二维分离:切换至不同品牌C18或HILIC、离子交换柱,进行脱盐处理或基于差异化色谱机理对捕获馏分二次分离,从物理层面拆分一维无法分辨的共流出组分;
Ø 质谱鉴定:QTOF提供低误差精确质量数及MS/MS碎片信息,完成组分定性与杂质结构推测,实现“分离-鉴定”一体化。
2. 核心技术优势
2.1 分离能力升维:破解单峰假象
传统一维LC-MS依赖单一分离机理,易出现共流出混合峰。2D-UPLC-QTOF通过正交分离系统,使一维重叠组分在二维中实现有效拆分。例如某注射液杂质检测中,一维未分辨的未知杂质,经“第一维NH₂柱+第二维T3柱”二维系统分离后呈现独立色谱峰,直接证实主峰不纯。其峰容量为两维单独峰容量的乘积,远超一维UPLC,可高效处理强制降解产生的复杂杂质体系。
2.2 检测灵敏度提质:消除漏检风险
一维LC-MS中,高浓度主成分会强烈抑制杂质离子化,导致1%以下低含量杂质信号被掩盖。2D-UPLC-QTOF通过时间差分离规避该问题,杂质经二维分离后单独进入离子源,离子化效率提升10-100倍,结合QTOF高灵敏度特性,可稳定捕捉主成分0.05%以下的微量杂质信号,完全满足监管对微量杂质的考察要求。
2.3 证据等级升级:提供直接物证
针对CDE对共流出物的核心关切,该技术可提供不可辩驳的直接证据:若二维分离后主峰仍为单一对称峰,且前沿、峰顶、后沿质谱图完全一致,可近乎绝对确认主峰纯度;若出现多峰,可直接获取杂质纯净质谱图,通过精确质量数计算候选分子式,结合碎片信息推导降解途径,这是一维方法无法实现的核心优势。
2.4 杂质解析延伸:实现根源溯源
QTOF的高分辨能力可实现杂质结构鉴定与工艺溯源。在双特异性抗体表征中,通过精确分子量与肽图分析,可定位主成分降解产生的片段杂质结构;在某注射液研究中,通过鉴定加热降解产生的缩合杂质,为优化灭菌工艺提供直接技术依据,实现“发现杂质-解析根源-优化工艺”的闭环。
三、CDE发补应对典型案例
案例1:小分子化药峰纯度考察
某药品注射剂申报时,CDE以“强制降解实验注意考察主峰纯度”为由发补,要求通过质谱方法验证主峰纯度。技术方案搭建二维液相和高分辨质谱平台:第一维采用标准方法的C18柱捕获主峰前、中、后三段,第二维切换T3反相柱在线除盐,通过对切割的三段主峰进行QTOF一级和二级质谱分析,确认主峰质谱信号一致,证明主峰不存在共流出杂质的风险,顺利通过评审。
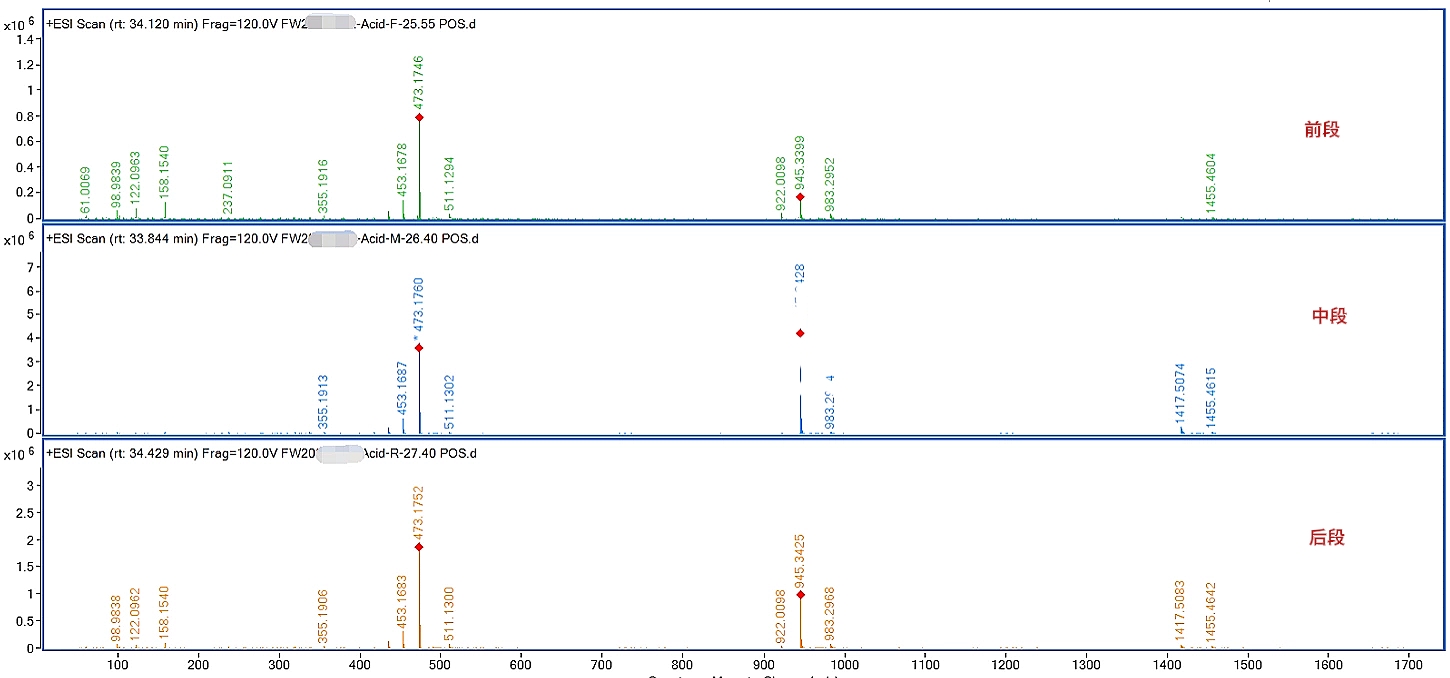
图2 主峰前、中、后三段一级质谱图比较
案例2:小分子化药新增未知杂质鉴定
某企业片剂药品申报时,因长期稳定性试验中出现0.07%新增杂质,未明确结构及安全性依据,收到CDE发补通知(符合《化学仿制药药学研究重大缺陷(试行)》第3条要求)。技术方案采用“第一维C18反相柱+第二维HILIC柱”二维系统配合QTOF检测:一维捕获主峰馏分后,二维分离出独立杂质峰,规避主成分离子抑制;QTOF测得精确质量数(误差3.2 ppm),确定候选分子式,结合MS/MS碎片推导为主成分降解产物;关联TTC计算(每日最大摄入0.35µg,符合0% TTC要求),出具毒理评估报告。最终10天内完成资料提交,零发补获批,较原计划提前3个月上市。
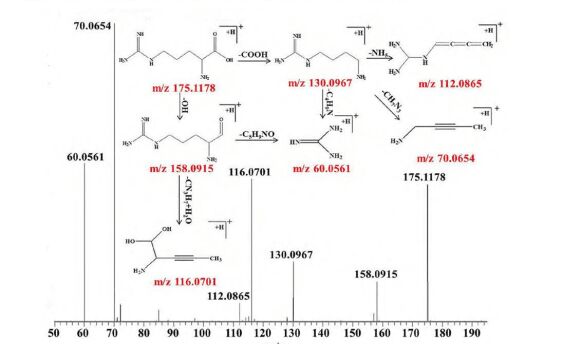
图3 杂质可能的裂解途径分析
四、项目研究报告核心要点
提交补充研究报告时,2D-UPLC-QTOF数据需聚焦以下三点,提升说服力:
1.二维色谱对比图:清晰展示第一维主峰区域与对应第二维分离色谱图的对比,若存在杂质,多峰特征一目了然,直观呈现分离效果;
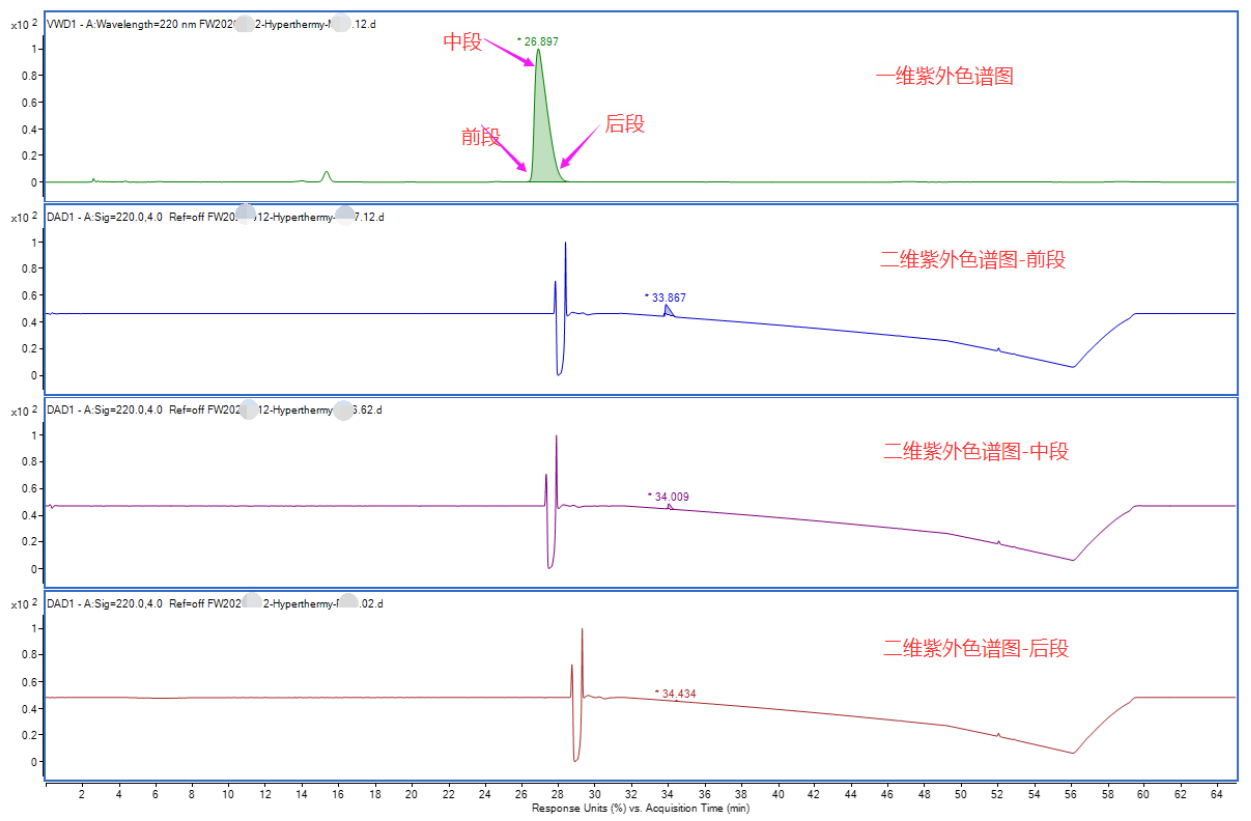
图4 第一维主峰与第二维色谱图的对比
2.高分辨质谱数据:针对二维分离出的每个峰,提供精确质量数、分子式及二级质谱碎片图,为杂质定性提供核心依据;
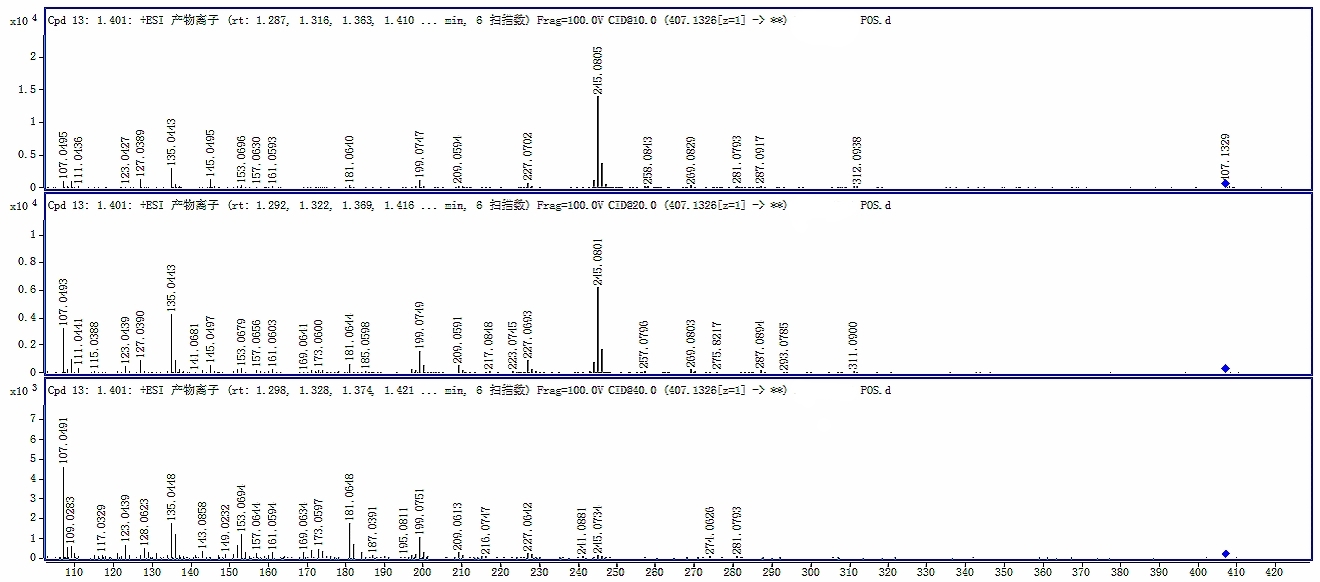
图5 化合物不同碰撞能下二级质谱碎片图

3.结论精准有力:发现杂质时,明确降解条件、杂质数量及关键质谱信息,同步说明原HPLC方法的分离有效性或优化方向;未发现杂质时,强调二维分离后主峰的单一性及质谱图一致性,证实分析方法的专属性与稳定性指示能力。
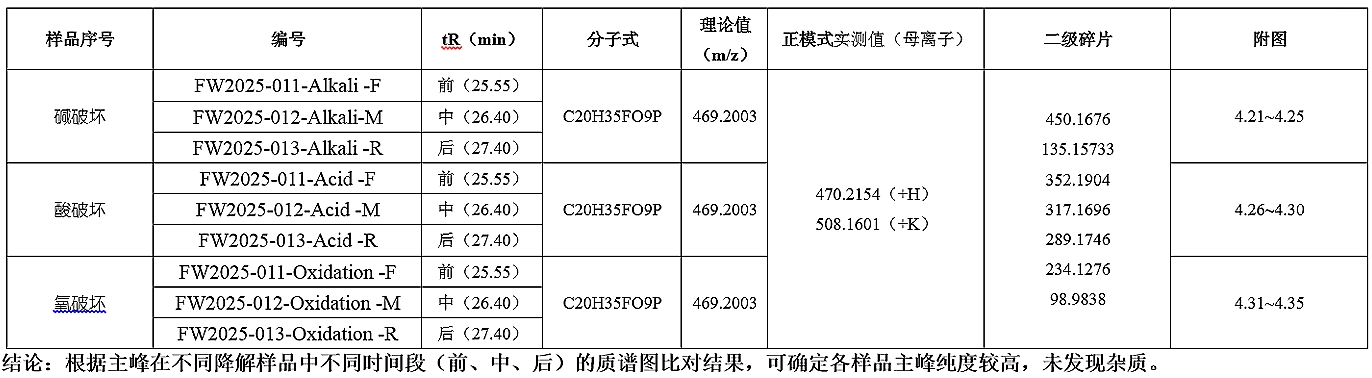
五、总结
2D-UPLC-QTOF技术融合二维色谱的高效分离能力与QTOF的精准鉴定优势,成为强制降解实验主峰纯度考察的“终极武器”,最高置信度回应CDE对色谱峰纯度的根本质疑,显著增强审评员对产品质量控制方法的信心。尽管该技术存在仪器成本高、操作及数据分析专业性强等问题,但在应对关键发补、为复杂制剂、生物药、ADC等高风险药物提供方法学验证数据时,是最可靠、权威的技术选择。建议在应对此类发补时,可与专业检测机构(如普思生物)合作,设计严谨实验方案,形成清晰逻辑链条与有力数据支撑,高效回应监管质疑,助力产品顺利通过审评。
[1]惠普公司. Peak purity analysis in HPLC and CE usdiode-array technology,1993.
成都普思生物是天然产物分离纯化及药学检测领域的领军企业,依托多年积累的技术优势和先进的仪器设备,为全球药物研发企业提供专业、可靠的技术服务与高质量产品。针对药物研发及注册申报过程中的关键发补环节普思生物能够提供清晰严谨的解决方案且能为复杂制剂、生物药、ADC(抗体药物偶联物)等高风险药物提供有力的数据支撑。
